- دمای ذوب: ۱۵۸.۶ درجه سانتیگراد
- دمای جوش: ۲۰۰ درجه سانتیگراد
- چگالی: ۲.۱۳ گرم بر سانتی متر مکعب
- حلال ها: آب، اتر، کربن تتراکلرید، بنزن، پروپانول، استون، اتانول، روغن تربانتین، تولوئن، کلروفرم، متانول و روغن زیتون
- سالیسیلیک اسید یک اسید مونوهیدروکسی بنزوئیک لیپوفیل، یک نوع اسید فنولیک و بتاهیدروکسی اسید است.
- این اسید آلی، بلورین و بیرنگ است و عمدتا در سنتز آلی استفاده میشود و به عنوان هورمون گیاهی عمل میکند.
- از متابولیسم سالیسین حاصل میشود.
- علاوه بر کاربرد به عنوان متابولیت مهم فعال آسپیرین که به عنوان پیش داروی سالیسیلیک اسید عمل میکند، احتمالا برای استفاده به عنوان ماده اولیه مهم در محصولات موضعی ضد آکنه شناخته شده است. نمکها و استرهای اسید سالیسیلیک با نام سالیسیلات شناخته میشوند.
- اسید سالیسیلیک از اسید آمینه فنیل آلانین بیوسنتز میشود. آن را میتوان از روش مستقل فنیل آلانین سنتز کرد.
- از روش صنعتی، سالیسیلات سدیم با استفاده از واکنش فنولات سدیم (نمک سدیم فنول) با دیاکسید کربن در فشار (۱۰۰ اتمسفر) و دمای بالا (۳۹۰ کیلوگرم) تولید میشود.
- از اسیدی کردن محصول این واکنش با اسید سولفوریک، سالیسیلیک اسید به دست میآید.
- همچنین توسط هیدرولیز آسپیرین (اسید استیل سالیسیلیک) یا متیل سالیسیلات با اسید یا باز قوی تهیه میشود.
کاربرد اسید سالیسیلیک
- اسید سالیسیلیک به عنوان دارو معمولا برای کمک به حذف لایه بیرونی پوست استفاده میشود.
- به این ترتیب، برای درمان زگیل، پسوریازیس، آکنه، عفونت قارچی، شوره سر، و پوست فلسی مورد استفاده قرار میگیرد.
- همانند سایر اسیدهای هیدروکسیلیک، اسید سالیسیلیک ماده اولیه مهم در بسیاری از محصولات مراقبت از پوست برای درمان درماتیت سبوریک، آکنه، پسوریازیس، میخچه ، پینه و زگیل است.
- اسید سالیسیلیک به عنوان نگهدارنده مواد غذایی، ضدباکتری و ضدعفونیکننده استفاده میشود.
- اسید سالیسیلیک در تولید داروهای دیگر از جمله اسید آمینواسلیکسیلیک ۴ و سولپیرید استفاده میشود.
- سالیسیلیک اسید یکی از مواد اولیه برای ساخت استیل سالیسیلیک اسید (آسپرین) بود. بیسموت سابسالیسیلات، نمک بیسموت و اسید سالیسیلیک، ماده فعال برای تسکین درد معد نقش ضد التهابی و همچنین آنتی اسیدی و آنتی بیوتیکی خفیف دارد.
- مشتقات دیگر این اسید مانند متیل سالیسیلات به عنوان مرهم رقیق برای تسکین درد مفاصل و عضلات و کولین سالیسیلات به طور موضعی برای تسکین درد آفت دهان استفاده میشوند. سالیسیلات سدیم یک فسفر مفید در محدوده طیفی فرابنفش با کارایی کوانتومی تقریبا مسطح برای طول موجهای بین ۱۰ تا ۱۰۰ نانومتر است.

راهنمای ایمنی کار با اسید سالیسیلیک
راهنمای حفاظت از دست ها
- بدلیل محاظت در برابر لبه های تیز،گرما و سرما، پاشش مواد شیمیایی و جابجایی مواد، استفاده از دستکش هنگام کار با مواد شیمیایی الزامی است.
- نوع دستکش مقاوم در برابر اسید باشد.
- قبل از استفاده از دستکش، از وضعیت و سالم بودن آن ها (سوراخ شدگی یا پارگی) اطمینان حاصل کنید. درصورت پاره شدن دستکش حین کار، بلافاصله آن را تعویض کنید و بلافاصله پس از درآوردن دستکش دست های خود را بشویید.
در صورت سوختگی پوست با مواد شیمیایی ابتدا لباس مصدوم را جدا کرده با دستمال تمیز محل را پاک کرده و بعد با آب ولرم محل را حداقل ۳۰ دقیقه در مورد اسیدها و تا ۲ ساعت در مورد مواد قلیایی آبکشی نمایید. - هنگام کمک رسانی به مصدوم از دستکش و ماسک استفاده کنید.
خطرات اسید سالیسیلیک
- اسید سالیسیلیک به عنوان یک عامل موضعی و بتا هیدروکسی اسید (بر خلاف آلفا هیدروکسی اسید) قادر به نفوذ و تجزیه چربیها و لیپیدها است،
- مقادیر زیاد آن باعث سوختگیهای شیمیایی پوست از درجه متوسط میشود، در حلالهایی مانند الکل، استون یا روغن ممکن است به روزنههای پوست آسیب برساند.
- اسید سالیسیلیک ۱۷٪ تا ۲۷٪ به صورت رنگ و ۲۰ تا ۵۰٪ به شکل گچ برای درمان زگیل و پینه در دسترس است
- و نباید برای صورت و درمان آکنه استفاده شود. حتی برای درمان زگیل، این محلول باید یک یا دو بار در روز استفاده شود، چراکه استفاده بیشتر ممکن است منجر به افزایش عوارض جانبی حتی بدون تاثیر بخشی شود.
- برخی افراد به اسید سالیسیلیک و ترکیبات مرتبط آن بسیار حساس هستند.
- اگر مقدار زیادی از پماد سالیسیلیک بروی سطح وسیعی از بدن استفاده شود، می تواند وارد خون شود و برای جلوگیری از عوارض بیشتر باید همودیالیز انجام شود.
پزشکی
اسید سالیسیلیک به عنوان یک دارو معمولاً برای برداشتن لایه بیرونی پوست استفاده می شود . به این ترتیب، برای درمان زگیل ، پسوریازیس ، آکنه ولگاریس ، کرم حلقوی ، شوره سر و ایکتیوز استفاده می شود . [11] [12] [13] [14]
مانند سایر اسیدهای هیدروکسی، اسید سالیسیلیک یک عنصر در بسیاری از محصولات مراقبت از پوست برای درمان درماتیت سبورئیک ، آکنه ، پسوریازیس ، پینه ، میخچه ، کراتوز پیلاریس ، آکانتوز نیگریکانس ، ایکتیوز و زگیل است. [15]
موارد استفاده در تولید
اسید سالیسیلیک به عنوان یک نگهدارنده مواد غذایی ، یک باکتری کش و یک ضد عفونی کننده استفاده می شود. [16] [17]
اسید سالیسیلیک در تولید سایر داروها، از جمله اسید 4-آمینو سالیسیلیک ، ساندولپیراید ، و لندتیماید (از طریق سالتامید ) استفاده می شود. [18]
اسید سالیسیلیک از دیرباز یک ماده اولیه کلیدی برای ساخت اسید استیل سالیسیلیک (آسپرین) بوده است. [9] آسپرین (اسید استیل سالیسیلیک یا ASA) با استری کردن فنولیک گروه هیدروکسیل اسید سالیسیلیک با گروه استیل از انیدرید استیک یا کلرید استیل تهیه میشود . [19] ASA استانداردی است که سایر داروهای ضد التهابی غیر استروئیدی ( NSAIDs ) با آن مقایسه می شوند. در دامپزشکی، این گروه از داروها عمدتاً برای درمان اختلالات اسکلتی عضلانی التهابی استفاده می شود. [20]
بیسموت ساب سالیسیلات ، نمکی از بیسموت و اسید سالیسیلیک، ماده فعال در داروهای تسکین دهنده معده مانند پپتو بیسمول ، ماده اصلی کائوپکتات است و “به دلیل اسید سالیسیلیک، اثر ضد التهابی نشان می دهد و همچنین به عنوان عمل می کند. یک آنتی بیوتیک ضد اسید و خفیف». [21]
مشتقات دیگر عبارتند از متیل سالیسیلات که به عنوان ماده ای برای تسکین درد مفاصل و ماهیچه ها استفاده می شود و کولین سالیسیلات که به صورت موضعی برای تسکین درد زخم های دهان استفاده می شود . [22] [23] اسید آمینوسالیسیلیک برای القای بهبودی در کولیت اولسراتیو استفاده می شود و به عنوان یک عامل ضد سل که اغلب همراه با ایزونیازید تجویز می شود، استفاده می شود . [24]
سالیسیلات سدیم یک فسفر مفید در فرابنفش خلاء محدوده طیفی است، با بازده کوانتومی تقریباً مسطح برای طول موجهای بین 10 تا 100 نانومتر. [25] در 420 نانومتر به رنگ آبی فلورسانس می شود. با پاشیدن محلول اشباع نمک در متانول و سپس تبخیر به راحتی روی سطح تمیزی آماده می شود. [ نیازمند منبع ]
مکانیسم عمل
اسید سالیسیلیک فعالیت آنزیمی COX-1 را تعدیل می کند تا تشکیل پروستاگلاندین های پیش التهابی را کاهش دهد. سالیسیلات ممکن است به طور رقابتی تشکیل پروستاگلاندین را مهار کند. اثرات ضدروماتیک (ضد التهاب غیر استروئیدی) سالیسیلات نتیجه مکانیسم های ضد درد و ضد التهابی آن است. [ نیازمند منبع ]
اسید سالیسیلیک به این صورت عمل می کند که باعث می شود سلول های اپیدرم راحت تر از بین بروند، از مسدود شدن منافذ جلوگیری می کند و فضا را برای رشد سلول های جدید باز می کند. اسید سالیسیلیک اکسیداسیون یوریدین-5-دی فسفوگلوکز (UDPG) را به صورت رقابتی با نیکوتین آمید آدنین دی نوکلئوتید و به صورت غیر رقابتی با UDPG مهار می کند. همچنین به طور رقابتی از انتقال گروه گلوکورونیل اسید یوریدین-5-فسفوگلوکورونیک به گیرنده فنلی جلوگیری می کند.
اثر تاخیری التیام زخم سالیسیلات ها احتمالاً به دلیل اثر مهاری آن بر سنتز موکوپلی ساکارید است. [6]
ایمنی
اگر غلظت های بالایی از پماد سالیسیلیک در درصد زیادی از سطح بدن استفاده شود، سطوح بالای اسید سالیسیلیک می تواند وارد خون شود و نیاز به همودیالیز برای جلوگیری از عوارض بیشتر دارد. [26]
تولید و واکنش های شیمیایی
بیوسنتز
اسید سالیسیلیک بیوسنتز از اسید آمینه فنیل آلانین می شود . در Arabidopsis thaliana ، می توان آن را از طریق یک مسیر مستقل از فنیل آلانین سنتز کرد.
سنتز صنعتی
سدیم سالیسیلات به صورت تجاری با تیمار سدیم فنولات (نمک سدیم فنل ) با دی اکسید کربن در فشار بالا (100 اتمسفر) و دمای بالا (115 درجه سانتیگراد) تهیه می شود – روشی که به عنوان واکنش کولبه اشمیت شناخته می شود . اسیدی شدن محصول با اسید سولفوریک اسید سالیسیلیک می دهد:
همچنین می توان آن را با هیدرولیز ( اسید آسپرین استیل سالیسیلیک) [27] یا متیل سالیسیلات (روغن زمستان سبز ) با اسید یا باز قوی تهیه کرد.
واکنش ها
با گرم شدن، اسید سالیسیلیک به فنیل سالیسیلات تبدیل می شود : [28] [9]
- 2 HOC 6 H 4 CO 2 H → C 6 H 5 O 2 C 6 H 4 OH + CO 2 + H 2 O
حرارت بیشتر زانتون می دهد . [9]
اسید سالیسیلیک به عنوان پایه مزدوج آن یک عامل کلات کننده است که میل ترکیبی به آهن (III) دارد. [29]
اسید سالیسیلیک به آرامی در دمای 200-230 درجه سانتیگراد به فنل و دی اکسید کربن تجزیه می شود: [30]
- C 6 H 4 OH (CO 2 H) → C 6 H 5 OH + CO 2
تاریخچه

بید از دیرباز برای اهداف دارویی استفاده می شده است. دیوسکوریدس که نوشتههایش برای بیش از 1500 سال بسیار تأثیرگذار بود [31] از «ایته» (که احتمالاً گونهای از بید بود) به عنوان درمانی برای «انسدادهای دردناک روده»، پیشگیری از بارداری، برای «کسانی که خون تف میدهند» استفاده کرد. برای از بین بردن پینه و میخچه و در خارج، به عنوان یک “بسته گرم برای نقرس”. ویلیام ترنر ، در سال 1597، این را تکرار کرد و گفت که پوست درخت بید، “سوزاندن به خاکستر، و غوطه ور شدن در سرکه، میخچه ها و سایر برآمدگی های پا و انگشتان را از بین می برد.” [32] برخی از این درمان ها ممکن است عملکرد اسید سالیسیلیک را توصیف کنند که می تواند از سالیسین موجود در بید به دست آید. با این حال، این یک افسانه مدرن است که بقراط از بید به عنوان مسکن استفاده می کند. [33]
بقراط ، جالینوس ، پلینی بزرگ و دیگران می دانستند که جوشانده های حاوی سالیسیلات می توانند درد را کاهش دهند و تب را کاهش دهند. [34] [35]
در اروپا و چین برای درمان این بیماری ها استفاده می شد. [36] این درمان در متون مصر باستان ، سومر و آشور ذکر شده است. [37]
و چروکی سایر بومیان آمریکا از دم کرده پوست آن برای تب و سایر اهداف دارویی استفاده می کنند. [38] در سال 2014، باستان شناسان ردپایی از اسید سالیسیلیک را بر روی قطعات سفالی قرن هفتم یافت شده در شرق مرکزی کلرادو شناسایی کردند. [39]
کشیش ادوارد استون ، جانشینی از چیپینگ نورتون، آکسفوردشایر ، انگلستان، در سال 1763 گزارش داد که پوست درخت بید در کاهش تب موثر است. [40]
عصاره ای از پوست درخت بید، به نام سالیسین ، پس از نام لاتین بید سفید ( Salix alba )، توسط آلمانی شیمیدان یوهان آندریاس بوخنر در سال 1828 جدا شد و نامگذاری شد. [41] مقدار بیشتری از این ماده در سال 1829 توسط هانری جدا شد. لرو، داروساز فرانسوی. [42] رافائل پیریا ، شیمیدان ایتالیایی ، توانست این ماده را به قند و جزء دوم تبدیل کند که در اثر اکسیداسیون به اسید سالیسیلیک تبدیل می شود. [43] [44] از گیاه علفزار ( ، به عنوان Spiraea ulmaria سالیسیلیک اسید نیز در سال 1839 توسط محققان آلمانی ulmaria که طبقه قبلا Filipendula شد) جدا شد . بندی می .
در سال 1874، پزشک اسکاتلندی، توماس مک لاگان، سالیسین را به عنوان درمانی برای روماتیسم حاد آزمایش کرد، با موفقیت قابل توجهی، همانطور که در لنست در سال 1876 گزارش کرد. [46] در همین حال، دانشمندان آلمانی سالیسیلات سدیم را با موفقیت کمتر و عوارض جانبی شدیدتری امتحان کردند. [47] [48]
در سال 1979، مشخص شد که سالیسیلات ها در دفاع القایی تنباکو در برابر ویروس موزاییک تنباکو نقش دارند . [49] در سال 1987، اسید سالیسیلیک بهعنوان سیگنالی که مدتها به دنبال آن بود، شناسایی شد که باعث میشود گیاهان گرمازا ، مانند زنبق وودو، Sauromatum guttatum ، گرما تولید کنند. [50]
منابع غذایی
اسید سالیسیلیک در گیاهان به صورت اسید سالیسیلیک آزاد و استرهای کربوکسیله و گلیکوزیدهای فنولیک آن وجود دارد. چندین مطالعه نشان می دهد که انسان سالیسیلیک اسید را در مقادیر قابل اندازه گیری از این گیاهان متابولیزه می کند. [51] نوشیدنی ها و مواد غذایی با سالیسیلات بالا شامل آبجو ، قهوه ، چای ، میوه ها و سبزیجات متعدد، سیب زمینی شیرین ، آجیل و روغن زیتون هستند. [52] گوشت، مرغ، ماهی، تخم مرغ، محصولات لبنی، شکر، نان و غلات محتوای سالیسیلات کمی دارند. [52] [53]
برخی از افراد با حساسیت به سالیسیلات های غذایی ممکن است علائم واکنش آلرژیک مانند آسم برونش ، رینیت ، اختلالات گوارشی یا اسهال را داشته باشند، بنابراین ممکن است نیاز به اتخاذ یک رژیم غذایی کم سالیسیلات داشته باشند. [52]
هورمون گیاهی
اسید سالیسیلیک یک فنلی فیتوهورمون است و در گیاهان با نقش هایی در رشد و نمو گیاهان، فتوسنتز ، تعرق و یون جذب و انتقال یافت می شود. [54] اسید سالیسیلیک در سیگنال دهی درون زا را واسطه می کند نقش دارد و دفاع گیاه در برابر پاتوژن ها . [55] ، در مقاومت به پاتوژنها (یعنی مقاومت اکتسابی سیستمیک با القای تولید پروتئینهای مرتبط با بیماریزایی و سایر متابولیتهای دفاعی ) نقش دارد. [56] نقش سیگنالدهی دفاعی SA به وضوح توسط آزمایشهایی که آن را از بین میبرند نشان میدهد: Delaney و همکاران. 1994، گافنی و همکاران. 1993، لاوتون و همکاران. 1995، و Vernooij و همکاران. 1994 هر کدام از Nicotiana tabacum یا Arabidopsis بیان کننده nahG برای سالیسیلات هیدروکسیلاز استفاده کردند. تلقیح پاتوژن سطوح بالایی از SA را ایجاد نکرد، SAR تولید نشد و هیچ ژن PR بیان در برگ های سیستمیک نشد. در واقع، آزمودنیها بیشتر مستعد ابتلا به پاتوژنهای بدخیم – و حتی به طور معمول غیر بیماریزا بودند. [54]
اسید سالیسیلیک به طور برون زا می تواند از طریق افزایش جوانه زنی بذر، گلدهی جوانه و رسیدن میوه به رشد گیاه کمک کند، اگرچه غلظت بیش از حد اسید سالیسیلیک می تواند به طور منفی این فرآیندهای رشدی را تنظیم کند. [57]
متیل استر فرار سالیسیلیک اسید، متیل سالیسیلات را تسهیل ، همچنین می تواند در هوا پخش شود و ارتباط گیاه و گیاه کند . [58] متیل سالیسیلات توسط روزنههای گیاه مجاور جذب میشود، جایی که میتواند پس از تبدیل مجدد به اسید سالیسیلیک، پاسخ ایمنی را القا کند. [59]
انتقال سیگنال
تعدادی از پروتئینها شناسایی شدهاند که با SA در گیاهان تعامل دارند، بهویژه پروتئینهای متصلکننده اسید سالیسیلیک (SABPs) و ژنهای NPR (Nonexpressor of pathogenesis related genes)، که گیرندههای احتمالی هستند. [60]
کریستالی بی رنگ است اسید سالیسیلیک یک کربوکسیلیک اسید سنتز می شود که به روش کلبه . به عنوان یک هورمون گیاهی شناخته می شود .
اگر به مقدار زیاد خورده شود سمی است، اما اگر به مقدار مناسب استفاده شود برای نگهداری مواد غذایی مفید است و به عنوان یک ضد عفونی کننده در خمیر دندان عمل می کند. گروه کربوکسیل ، COOH، به راحتی با الکل ها تولید واکنش می دهد و استر می کند . با استر که متانول (یا متیل سالیسیلات) است متیل سالیسیلات جزء ضروری Gaultheria procumbens و بید سفید (Salix alba) است. غذاهایی که به طور طبیعی سرشار از اسید سالیسیلیک هستند عبارتند از زردآلو (3 میلی گرم در 100 گرم)، توت سیاه و قرمز (5 میلی گرم در 100 گرم)، کاسنی (1 میلی گرم در 100 گرم)، پرتقال (2.4 میلی گرم در هر 100 گرم)، آناناس (2 میلی گرم در 100 گرم) و تمشک (5 میلی گرم در 100 گرم).
با جایگزینی هیدروکسیل فنولیک با یک استیل، اسید استیل سالیسیلیک ، ماده موثره شناخته شده آسپرین به دست می آید.
اسید سالیسیلیک جزء ضروری برخی از محصولات درمان پوست و به ویژه برای درمان آکنه ، کراتوز پیلاریس و زگیل است. همچنین در موارد پسوریازیس به منظور رفع پوسته پوسته شدن و در نتیجه تسهیل درمان موضعی قابل استفاده است.
- 1 نقش یک دارو
- 2 بیوسنتز
- 3 نقش به عنوان یک هورمون گیاهی
- 4 ترکیبات مشابه
- 5 توجه
- 6 کتابشناسی
- 7 صدا همبستگی
- 8 پروژه های دیگر
- 9 پیوندهای خارجی
نقش یک دارو
خواص درمانی اسید سالیسیلیک از زمان های قدیم شناخته شده است [2] به طوری که این ماده از گیاه بید استخراج می شد که نام آن از آن گرفته شده است. از قرن نوزدهم عصاره سالیسین ، گلیکوزیدی که از گلوکز و اسید سالیسیلیک تشکیل میشود، در پزشکی به عنوان یک ضد التهاب در درمان آرتریت روماتوئید استفاده میشود . متعاقباً مشتقات متعددی سنتز شدهاند که کلاس سالیسیلاتها را تشکیل میدهند که شناختهشدهترین آنها اسید استیل سالیسیلیک (آسپرین) است.
علاوه بر این، سالیسیلیک اسید در پوست برای درمان پسوریازیس استفاده می شود. این ترکیب دارای خواص کراتولیتیک است : در محلول الکلی 6 درصد روی سطح قرار می گیرد تا تمیز شود. پس از چند دقیقه تبخیر قسمت الکلی و رسوب اسید سالیسیلیک وجود دارد که اثر خود را بر روی کراتینوسیت اعمال می کند.
بیوسنتز
این اسید در سلول های گیاهی از فنیل آلانین ایجاد می شود که به اسید ترانس سینامیک تبدیل می شود . این اسید از طریق اکسیداسیون احیا کننده یا غیر احیا تبدیل می به اسید بنزوئیک کننده به شکل گلیکوزیله شود. شکل گلیکوزیله در گیاه غیرفعال است و به لطف آنزیم بنزوئیک اسید هیدروکسیلاز به اسید سالیسیدیک تبدیل میشود که میتواند به اسید سالیسیدیک – گلوکز تبدیل شود ، یعنی شکل غیر فعالی که معمولاً در داخل گیاه یافت میشود. علاوه بر این، به نظر می رسد برخی از مطالعات تأیید می کنند که مسیرهای بیوسنتزی اسید سالیسیلیک وجود دارد که شامل تولید اسید بنزوئیک نمی شود. [ بدون منبع ]
اسید سالیسیلیک در داخل سبزی ثابت نیست، بلکه در امتداد عروق حرکت می کند. [ بدون منبع ]
نقش به عنوان یک هورمون گیاهی
اسید سالیسیلیک به عنوان یک هورمون گیاهی [3] تنفس مقاوم به سیانید ( اکسیداز جایگزین ) را به ویژه در گیاهان خانواده آراسه تحریک می کند. فعالسازی آن شامل تولید گرما میشود که مواد فراری مانند ایندولها و/یا پلیآمینها را برای گردهافشانی انتوموفیل آزاد میکند . را تعیین می کند ، مسئول مقاومت در برابر خانواده پاتوژناز همچنین با القای تولید آنزیم های پاتوژن (PRP) که مقاومت اکتسابی سیستمیک (SAR – Systemic Acquired Resistance ) های گیاهی است [4] .
اسید مستقیماً مسئول پاسخ SAR در سبزی نیست، اما اگر تولید نشود، فعال نمی شود. به طور خاص، پس از انجام آزمایشهایی بر روی جهشیافتههای EDS ، یعنی جهشیافتههای حساس به پاتوژن که در آن مشخص شد ژن NIM1 به دلیل جهشیافته بودن، فعال نشده است، این امکان وجود داشت . همچنین ژن NPR1 که پروتئین NPR1 را کد می کند که با میل ترکیبی بالا به پروتئین های TGA متصل می شود، دخیل است. NPR1-TGA به دایمر عنوان یک فعال کننده برای ژن PR1 عمل می کند که در ایجاد اسید سالیسیلیک و خود TGA نقش دارد. بنابراین افزایش غلظت NPR1 منجر به افزایش غلظت اسید سالیسیلیک می شود.
ترکیبات مشابه
در آزمایشگاه، ترکیبات مشابهی از اسید سالیسیلیک ساخته شده است، مانند 2،6 دی کلروایزونیکوتینیک اسید (INA) و بنزوتیازول ها (BTH)، که قادر به فعال کردن پاسخ SAR در گیاه در غیاب کامل SA درون زا هستند.
| |||
 | |||
| نام ها | |||
|---|---|---|---|
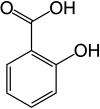
| نام ترجیحی IUPAC 2-هیدروکسی بنزوئیک اسید [1] | |||
| شناسه ها | |||
شماره CAS |
| ||
مدل سه بعدی ( JSmol ) |
| ||
| ChEBI |
| ||
| محفظه – اتاق |
| ||
| ChemSpider |
| ||
| بانک دارو |
| ||
| کارت اطلاعات ECHA | 100.000.648 | ||
| شماره EC |
| ||
IUPHAR/BPS |
| ||
| KEGG |
| ||
PubChem CID |
| ||
| شماره RTECS |
| ||
| مقداری |
| ||
داشبورد CompTox ( EPA ) |
| ||
InChI | |
لبخند می زند | |
| خواص | |
|---|---|
فرمول شیمیایی | C7H6O3 _ _ _ _ _ |
| جرم مولی | 138.122 گرم در مول |
| ظاهر | کریستال های بی رنگ تا سفید |
| بو | بی بو |
| تراکم | 1.443 گرم بر سانتی متر 3 (20 درجه سانتی گراد) [2] |
| نقطه ذوب | 158.6 درجه سانتی گراد (317.5 درجه فارنهایت؛ 431.8 K) |
| نقطه جوش | 200 درجه سانتیگراد (392 درجه فارنهایت؛ 473 K) تجزیه می شود [3] 211 درجه سانتی گراد (412 درجه فارنهایت؛ 484 کلوین) در 20 میلی متر جیوه [2] |
تصعید شرایط | در دمای 76 درجه سانتیگراد تعالی می یابد [4] |
حلالیت در آب |
|
| انحلال پذیری | محلول در اتر ، CCl4 پروپانول ، بنزن ، استون ، اتانول ، ، ، روغن سقز تولوئن |
| حلالیت در بنزن |
|
| حلالیت در کلروفرم |
|
| حلالیت در متانول |
|
| حلالیت در روغن زیتون | 2.43 گرم / 100 گرم (23 درجه سانتیگراد) [3] |
| حلالیت در استون | 39.6 گرم در 100 گرم (23 درجه سانتیگراد) [3] |
| ورود به سیستم P | 2.26 |
| فشار بخار | 10.93 mPa [4] |
| اسیدیته p Ka ) ( |
|
| UV-vis (λ max ) | 210 نانومتر، 234 نانومتر، 303 نانومتر (4 میلی گرم در دسی لیتر در اتانول) [4] |
حساسیت مغناطیسی (χ) | -72.23· 10-6 سانتی متر 3 / مول |
ضریب شکست ( n D ) | 1.565 (20 درجه سانتیگراد) [2] |
لحظه دوقطبی | 2.65 D |
| ترموشیمی | |
آنتالپی STD از تشکیل (Δ f H ⦵ 298 ) | -589.9 کیلوژول بر مول |
آنتالپی STD از احتراق (Δ c H ⦵ 298 ) | 3.025 MJ/mol [7] |
| فارماکولوژی | |
کد ATC | A01AD05 ( WHO ) B01AC06 ( WHO ) D01AE12 ( WHO ) N02BA01 ( WHO ) S01BC08 ( WHO ) |
| خطرات | |
| ایمنی و بهداشت شغلی (OHS/OSH): | |
خطرات چشمی | تحریک شدید |
خطرات پوستی | تحریک خفیف |
| GHS برچسبگذاری : [8] | |
پیکتوگرام ها |   |
کلمه سیگنال | خطر |
اظهارات خطر | H302 ، H318 |
اظهارات احتیاطی | P280 ، P305+P351+P338 |
| NFPA 704 (الماس آتشین) |
2 1 0 |
| نقطه اشتعال | 157 درجه سانتی گراد (315 درجه فارنهایت؛ 430 کلوین) فنجان بسته [4] |
خود اشتعال درجه حرارت | 540 درجه سانتیگراد (1004 درجه فارنهایت؛ 813 K) [4] |
| دوز یا غلظت کشنده (LD، LC): | |
LD 50 ( دوز متوسط ) | 480 میلی گرم بر کیلوگرم (موش، خوراکی) |
| برگه داده های ایمنی (SDS) | MSDS |
| ترکیبات مرتبط | |
ترکیبات مرتبط | متیل سالیسیلات ، اسید بنزوئیک ، فنل ، آسپرین ، 4-هیدروکسی بنزوئیک اسید منیزیم سالیسیلات ، کولین سالیسیلات ، بیسموت ساب سالیسیلات ، اسید سولفوسالیسیلیک ، سالیسیلات سنتاز |
به جز مواردی که غیر از این ذکر شده است، داده ها برای مواد در حالت استاندارد آنها (در دمای 25 درجه سانتیگراد [77 درجه فارنهایت]، 100 کیلو پاسکال) ارائه می شود. ارجاعات صندوق اطلاعات | |
سالیسیلیک اسید یا 2-هیدروکسی بنزوئیک اسید
یک آلی ترکیب معطر ، یکی از سه ایزومر هیدروکسی بنزوئیک اسید است که از یک حلقه بنزن جایگزین شده توسط یک گروه کربوکسیل ( اسید بنزوئیک ) و یک گروه هیدروکسیل ( فنل ) در موقعیت ارتو تشکیل شده است. این یک جامد کریستالی بی رنگ است که به طور طبیعی در گیاهان خاصی یافت می شود، از جمله بید سفید (که نام خود را از آن گرفته است) و اسپیرا کاذب (که نام منسوخ اسید اسپیریک از آن گرفته شده است ) که به عنوان دارو و پیش ساز اسید استیل سالیسیلیک ، آسپرین استفاده می شود. .
رخداد طبیعی
اسید سالیسیلیک به طور طبیعی توسط گیاهان خاصی (مانند شیرین علفزار یا بید ) سنتز می شود، به ویژه در میوه ها ، به شکل استری شده متیل سالیسیلات یافت می شود. این می تواند به عنوان یک سیگنال هورمونی عمل کند که در برخی موارد می تواند گرمازایی گیاه 8 .
خواص
مصرف در مقادیر زیاد، یک محصول سمی است ، اما در مقادیر کمتر به عنوان نگهدارنده مواد غذایی و ضد عفونی کننده استفاده می شود.
خواص پزشکی اسید سالیسیلیک برای مدت طولانی شناخته شده است، به ویژه به دلیل اثر آن در برابر تب . به طور عمده از بید ، سالیکس در لاتین که نام خود را از آن گرفته است، استخراج شده است. در مبارزه با تب، اکنون با داروهای موثرتر دیگری مانند آسپرین (که یک مشتق آن است) یا پاراستامول جایگزین می شود .
این دیگر برای اثر تسکین دهنده ( ضد درد ) استفاده نمی شود و علاوه بر یک ماده فعال دیگر در بسیاری از محصولات پوستی یافت می شود. به عنوان مثال در درمان آکنه ، زگیل یا هیپرهیدروزیس استفاده می شود.
سنتز و خواص شیمیایی
گروه کربوکسیلیک اسید (-COOH) می تواند با یک الکل زیادی بدهد واکنش دهد و استرهای . گروه هیدروکسیل می تواند با اسید استیک واکنش داده و اسید را تشکیل استیل سالیسیلیک یا آسپرین دهد.
در صنعت، اسید سالیسیلیک توسط واکنش کلبه سنتز می شود :
سنتز
اسید سالیسیلیک با یون سالیسیلات یک جفت اسید/باز با فرمول C 6 H 4 OHCOOH / C 6 H 4 OHCOO – تشکیل می دهد.
سمیت
مقاله مرتبط: حساسیت به سالیسیلات .
بخارات تحریک کننده غشاهای مخاطی چشم و تنفسی. محصول قابل اشتعال
دخالت در مقاومت سیستمیک اکتسابی
تجمع اسید سالیسیلیک، تولید شده در نتیجه شناسایی پاتوژن، برای فعال شدن مقاومت سیستمیک اکتسابی 9 . بنابراین، بیوسنتز اسید سالیسیلیک زمانی افزایش می یابد که گیاه یک پاتوژن ویروسی یا غیر ویروسی را تشخیص دهد. این تجمع باعث تحریک مقاومت در برابر تکثیر ویروس و تکثیر درون سلولی آن می شود. به لطف این مقاومت، عفونت کمتر احتمال دارد که سیستمیک شود. و با این حال، برخی از ویروس ها (به عنوان مثال: ویروس موزاییک تنباکو ) بیوسنتز اسید سالیسیلیک را در میزبان تحریک می کنند. این پدیده نشان می دهد که اسید سالیسیلیک تکثیر ویروس را تعدیل می کند و بنابراین از نکروز و سایر علائم تشدید شده در گیاه جلوگیری می کند. از طریق نکروز، ذرات ویروس در بافت نکروز غیرفعال می شوند و ویروس قادر به انتشار در گیاه نخواهد بود. به عبارت دیگر، ویروس سنتز اسید سالیسیلیک را به منظور کند کردن تکثیر آن ترویج می کند. با کاهش سرعت تکثیر آن، علائم گیاه تعدیل می شود و ویروس بهتر می تواند پخش و تکثیر شود. 10 .
اسید سالیسیلیک (به انگلیسی: Salicylic acid ، مشتق شده از کلمه لاتین “willow” salix )، همچنین با نامهای اسید سالیسیلیک ، اسید o-هیدروکسی بنزوئیک ، اسید 2-هیدروکسی بنزوئیک نیز شناخته میشود . اسید سالیسیلیک به راحتی در اتانول ، اتر ، کلروفرم ، بنزن ، استون و سقز در 20 درجه سانتی گراد محلول است، اما به راحتی در آب حل نمی شود. حلالیت آن 0.2 گرم در 100 میلی لیتر است [1] . در طبیعت در پوست درخت بید ، برگ های مروارید سفید و توس کوهی وجود دارد. اسید سالیسیلیک یک اسید آلی است که می تواند از سالیسین متابولیزه شود. این به طور گسترده در سنتز آلی استفاده می شود و همچنین یک هورمون گیاهی است . اسید سالیسیلیک ساختار و کارایی مشابه آسپرین (اسید استیل سالیسیلیک) دارد و همچنین می تواند برای درمان آکنه استفاده شود [2] .
تاریخچه
در حدود قرن پنجم قبل از میلاد، یونانی ، پزشک بقراط ، ثبت کرد که می توان از پودر تلخی که از پوست درخت بید استخراج می شود برای تسکین درد و کاهش تب استفاده کرد. این روش در سومر , لبنان و آشور اسناد باستانی نیز دیده می شود . چروکی ها و دیگر بومیان آمریکا سنت استفاده از دم کرده پوست برای درمان تب دارند [3] و از پوست داخلی گیاه برای ساختن دارو و تسکین درد استفاده می کردند. در سال 1763، یک روحانی انگلیسی به نام ادوارد (ادموند) استون خاطرنشان کرد که پوست درخت بید در کاهش تب موثر است. [4]
در سال 1828، هانری لو روکس، داروساز فرانسوی و رافائل پیریا، شیمیدان ایتالیایی، ماده موثره را از پوست درخت بید استخراج کردند و بید سفید نام لاتین را سالیسین گذاشتند. پیریا با تجزیه این ماده اسید سالیسیلیک به دست آورد.
در سال 1839، محققان آلمانی نیز ulmaria Filipendula استخراج کردند. اسید سالیسیلیک را از اگرچه عصارههای آنها اثر درمانی یکسانی دارند، اما عوارض جانبی بر روی سیستم گوارشی نیز دارند، مانند ایجاد التهاب معده، خونریزی، اسهال و مرگ در صورت مصرف در دوزهای بالا.
هورمون های گیاهی
اسید سالیسیلیک یک هورمون فنلی است که می تواند رشد و نمو گیاهان را تنظیم کند و همچنین فتوسنتز ، تعرق و یون جذب و حمل و نقل گیاهان را تنظیم می کند. اسید سالیسیلیک همچنین می تواند باعث تمایز سلول های گیاهی تولید و کلروپلاست شود. اسید سالیسیلیک همچنین به عنوان یک سیگنال درون زا پاتوژن ها در دفاع گیاه در برابر شرکت می کند [5] ، با القای بافت ها برای تولید پروتئین های مرتبط با فرآیند بیماری، و زمانی که بخشی از گیاه توسط یک عامل بیماری زا آلوده می شود، مقاومت در قسمت های دیگر ایجاد می شود. این سیگنال همچنین می تواند از طریق تشکیل متیل سالیسیلات فرار بین گیاهان مختلف منتقل شود. [6]
دارویی
اسید سالیسیلیک در زمان های قدیم برای تسکین درد و تب و همچنین اثر ضد التهابی استفاده می شده است.
در طب مدرن، متیل سالیسیلات نیز برای تسکین درد مفاصل و عضله استفاده می شود؛ کولین سالیسیلات به طور گسترده ای برای درمان زخم های دهان استفاده می شود.

مشابه AHA ها (آلفا هیدروکسی اسیدها)، اسید سالیسیلیک یک ماده لایه بردار کلیدی در بسیاری از محصولات مراقبت از پوست است و هنگامی که در داروسازی استفاده می شود، می تواند آکنه ، درماتیت سبورئیک ، پسوریازیس ، میخچه و کراتوز پیلاریس را درمان کند. [8] هایپرتروفیک استفاده می شود هنگامی که برای از بین بردن پیله ، غلظت معمولی آن 6% پماد آسپرین-وازلین است که به مدت 1 ساعت روی ناحیه مالیده می شود و سپس شسته می شود.
اسید سالیسیلیک برای مصارف خارجی خاصیت ضد باکتریایی در برابر میکروارگانیسم ها دارد و قدرت ضدعفونی کنندگی آن نزدیک به فنل است. اسید سالیسیلیک می تواند کوتین را حل کند و غلظت فرآورده های آن متفاوت است و اثرات دارویی آن متفاوت است:
- 1 تا 3 درصد دارای اثرات کراتینوژنیک و ضد خارش هستند؛ شامپوهای رایج بدون نسخه (OTC) اسید سالیسیلیک حاوی 3 درصد اسید سالیسیلیک هستند.
- 5 تا 10 درصد دارای اثر کراتولیتیک است که می تواند چسب بین سلول های سنگفرشی متصل در لایه شاخی را حل کند، به طوری که شاخی می تواند شل شود و پوسته پوسته شود و همچنین می تواند اثرات ضد قارچی ایجاد کند (به دلیل حذف لایه شاخی و رشد). قارچ ها مهار می شود، اسید سالیسیلیک می تواند به سایر داروهای ضد قارچی کمک کند تا نفوذ کنند و رشد باکتری ها را مهار کنند).
- 25 درصد غلظت اثر خورنده دارد و می تواند پینه هایپرتروفیک را از بین ببرد. برای سبوره، درماتیت سبورئیک ، میکوز سطحی، زگیل، میخچه، پینه و هیپرکراتوز موضعی مناسب است.
کاربردهای دیگر
- اگرچه دوزهای زیاد اسید سالیسیلیک برای بدن انسان مضر است، اسید سالیسیلیک اغلب به عنوان یک نگهدارنده در غذا و یک در خمیر دندان عامل ضد باکتری استفاده می شود. برای برخی از افرادی که به اسید سالیسیلیک حساسیت دارند، قرار گرفتن در معرض دوزهای کوچک ممکن است مضر باشد.
- متداول فرابنفش خلاء سالیسیلات سدیم یک فسفر است که می تواند فلورسانس با طول موج 420 نانومتر منتشر کند. [9]
- لینیمنت متیل سالیسیلات درد مفاصل و عضلات را تسکین می دهد. [درخواست منبع]
بیسموت ساب سالیسیلات یک داروی رایج معده است که برای درمان اسهال ، حالت تهوع، سوزش سر دل و نفخ استفاده می شود. همچنین یک آنتی بیوتیک خفیف است.
کولین سالیسیلیک اسید به صورت موضعی برای درمان زخم های دهان استفاده می شود.
امنیت
اسید سالیسیلیک می تواند باعث درماتیت تماسی شود. پس از مصرف و جذب در مقیاس بزرگ، علائم مسمومیت سیستمیک با اسید سالیسیلیک ممکن است ظاهر شود ، مانند سرگیجه ، گیجی، سردرگمی ذهنی، تنگی نفس، وزوز گوش مداوم، سردرد شدید یا مداوم ، و درد گزگز.
افراد مبتلا به دیابت ، محیطی یا نوزادان ، بیماری عروق از کرم یا پماد اسید سالیسیلیک 25 تا 60 درصد، گچ اسید سالیسیلیک 15 تا 50 درصد، ژل سالیسیلیک اسید 17 درصد، محلول سالیسیلیک اسید 13.6 تا 26 درصد باید به دقت استفاده کنند. ممکن است باعث کاندیدیال التهاب یا زخم یا حتی مرگ شود؛ از اسید سالیسیلیک 25 تا 60 درصد کرم یا پماد، اسید سالیسیلیک 40 تا 50 درصد گچ برای درماتیت یا عفونت پوست استفاده کنید، همچنین باید توجه شود.
اسید سالیسیلیک می تواند فعالیت پرستین را در غشای قاعده جانبی سلول های مویی خارجی مهار کند ، بنابراین سمیت گوش دارد. [10] [11] ممکن است باعث ناشنوایی موقت در بیماران مبتلا به کمبود روی شود. این یافته بر اساس آزمایشات بالینی روی موش ها است. تزریق سالیسیلیک اسید به موش های فاقد روی می تواند باعث ناشنوایی شود، در حالی که تزریق همزمان محلول روی می تواند ناشنوایی را درمان کند. تزریق محلول منیزیم به موشهای دارای کمبود روی، ناشنوایی اسید سالیسیلیک را درمان نکرد.
هیچ مطالعه خاصی در مورد اثرات اسید سالیسیلیک بر بارداری وجود ندارد. اسید سالیسیلیک خوراکی (یا آسپرین) در طول سه ماهه اول خطر ناهنجاری های جنینی را افزایش نمی دهد، اما مصرف آن در سه ماهه سوم ممکن است باعث خونریزی داخل جمجمه جنین شود [12] [منبع کامل مورد نیاز است] . اسید سالیسیلیک موضعی حتی در اواخر بارداری نیز عوارض جانبی ایجاد نمی کند. بسیاری از داروهای پوستی موضعی حاوی اسید سالیسیلیک هستند و هیچ گزارشی از خطر تراتوژنیک اسید سالیسیلیک موضعی وجود ندارد. [13]
اسید سالیسیلیک بیش از حد می تواند منجر به مسمومیت با اسید سالیسیلیک شود که از نظر بالینی به صورت اسیدوز متابولیک و آلکالوز تنفسی ظاهر می شود. میزان موربیدیتی بیماران حاد 16 درصد و میزان مرگ و میر 1 درصد بود. [14]
برخی از افراد به اسید سالیسیلیک و مشتقات آن حساسیت دارند.
FDA استفاده از ضد آفتاب را با محصولات مراقبت از پوست که حاوی اسید سالیسیلیک (یا هر آنتی اکسیدان دیگری) هستند، توصیه می کند. [15]
اگرچه هیچ داده ای وجود ندارد که نشان دهد استفاده از اسید سالیسیلیک می تواند باعث سندرم ری شود ، بنیاد ملی سندرم ری توصیه می کند که کودکان و نوجوانان (زیر 16 سال) استفاده از اسید سالیسیلیک و آسپرین را به حداقل برسانند. [16]
سنتز
در موجودات زنده سالیسیلیک اسید را می توان از فنیل آلانین سنتز کرد .
تولید صنعتی سالیسیلیک اسید عبارت است از طریق واکنش کلبر-اشمیت از سنتز نمک سدیم اسید سالیسیلیک با فنل و دی اکسید کربن در دمای بالا (390K) و فشار بالا (100 اتمسفر) و سپس اسیدی کردن آن با اسید سولفوریک برای بدست آوردن سالیسیلیک. اسید.