پلی الکترولیت چیست؟
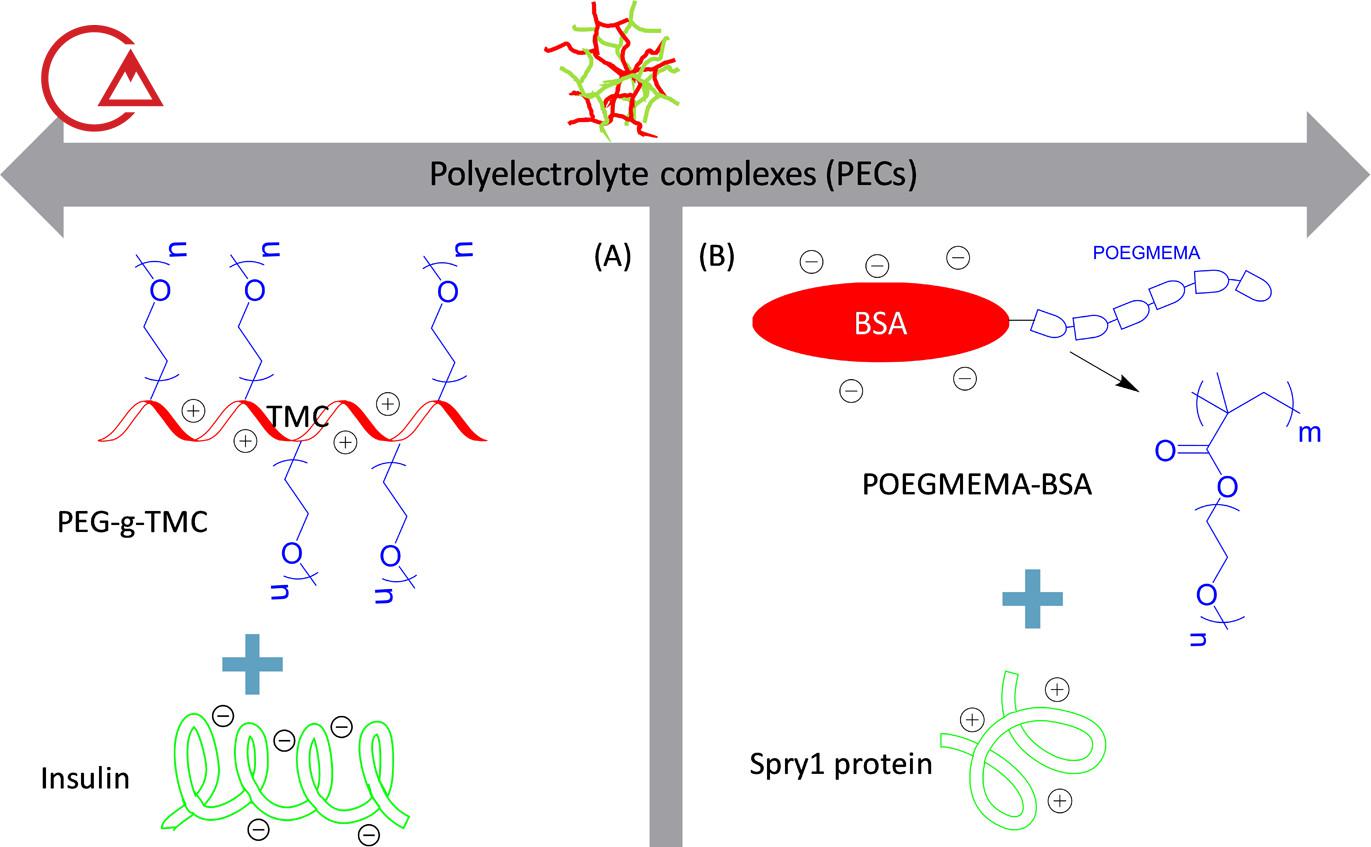
پلی الکترولیت (PEC) یک اصل ساده اما بسیار جالب با اهمیت قابل توجهی در تحویل پروتئین را نشان می دهد. فاز معکوس تولید میشوند میکروامولسیون. این فرآیند اغلب مستلزم استفاده از سمی حلال های آلی ، گرما، هم زدن شدید یا مواد شیمیایی است که ممکن است پایداری و زیست سازگاری محصولات نهایی را به خطر بیندازند . با این حال، فرآیند ساخت PEC در اندازه نانو آسان است، و امروزه جایگزین جذابی برای فرمولهای نانوذرات معمولی است، که از انفجار اخیر ادبیات در مورد استفاده از PEC در تحویل پروتئین [2،4-8] . به طور کلی سه روش برای ساخت PEC وجود دارد که در شکل 7.1 است.
نیروی محرکه اصلی تشکیل PEC برهمکنش الکترواستاتیکی (کولومبیک) بین پلی الکترولیت های دارای بار مخالف است. با این حال، برهمکنشهای بین مولکولی دیگر، مانند پیوند هیدروژنی، آبگریز و نیروهای واندروالسی گزارش شده است که نقش مهمی در تشکیل این دارند . از آنجایی که تشکیل PEC صرفاً بر اساس برهمکنش غیرکووالانسی است و عمدتاً توسط برهمکنش کولمبی انجام می شود، تعدادی از عوامل وجود دارد که می تواند بر شکل گیری و پایداری آن تأثیر بگذارد. وزن مولکولی پلی الکترولیت ها (PE)، نسبت های استوکیومتری و غلظت PE و پروتئین ها، قدرت یونی و pH محلول و دما همگی بر ماهیت تشکیل کمپلکس تأثیر خواهند داشت که متعاقباً بر پایداری و کارایی فرمولاسیون نهایی تأثیر می گذارد.
متون فراوانی وجود دارد که استفاده از پلی الکترولیت و منعقد کننده ها را برای تحویل پروتئین گزارش می کند، که کیتوزان رایج ترین پلی الکترولیت مورد استفاده گزارش شده است. کیتوزان در حالت بومی خود قبلاً به طور گسترده در ادبیات بررسی شده است [4-6،8] و تا حدی توسط مشتقات آن، یعنی نمک های آمونیوم چهارتایی و تیومرها جایگزین شده است. همچنین گزارش های محدودی در مورد استفاده از پلی الکترولیت های آمفیفیل در این منطقه وجود دارد [17،24-26] . بنابراین هدف این فصل بررسی استفاده از پلی الکترولیتهای آمفیفیل و کیتوزان اصلاحشده شیمیایی برای انتقال پروتئین و پپتیدها به دستگاه گوارش و بحث در مورد اینکه چگونه تغییرات شیمیایی بر دو چالش مهم در تحویل پروتئین/پپتید خوراکی تأثیر گذاشته است، است. محافظت در برابر تخریب آنزیمی دستگاه گوارش غشای مخاطی .
| نمونه های الف | PEC b (g) | 2.5 M KBr (mL) | H 2 O (mL) | [KBr] c (M) |
|---|---|---|---|---|
| PEC 1.33 | 1.5 | 8.4 | 6.6 | 1.33 |
| PEC 1.43 | 1.5 | 9.0 | 6.0 | 1.43 |
| PEC 1.46 | 1.5 | 9.3 | 5.7 | 1.46 |
| PEC 1.51 | 1.5 | 9.6 | 5.4 | 1.51 |
| PEC 1.56 | 1.5 | 9.9 | 5.1 | 1.56 |
| PEC 1.60 | 1.5 | 10.2 | 4.8 | 1.60 |
| PEC 1.65 | 1.5 | 10.5 | 4.5 | 1.65 |
| PEC 1.69 | 1.5 | 10.8 | 4.2 | 1.69 |
| PEC 1.73 | 1.5 | 11.1 | 3.9 | 1.73 |
| PEC 1.78 | 1.5 | 11.4 | 3.6 | 1.78 |
| PEC 1.84 | 1.5 | 11.7 | 3.3 | 1.84 |
| PEC 1.88 | 1.5 | 12.0 | 3.0 | 1.88 |
فروش پلی الکترولیت
پلی الکترولیت توسط فعل و انفعالات ارتباطی بین پلی الکترولیت که منجر به تشکیل یک فاز متراکم پلیمری ماکروسکوپی و یک فاز رقیق پلیمری با کاربرد در پوشش ها، چسب ها و تصفیه غشاهای فراتر از جداسازی فاز در مقیاس ماکرو، سنتز پلیمری توسعه بیشتر میسلها خودساخته مبتنی بر کمپلکس پلیالکترولیت (PEC) با کاربرد در بیوتکنولوژی را ممکن کرده است. جالب توجه است، پیشنهاد شده است که مکانیسمهای مشابه کمپلکسسازی پلیالکترولیت، تشکیل میعانات بیولوژیکی را تحریک میکند که نقش ضروری در بیوژنز سلولی دارند. مسیرهای شکل گیری و عملکرد این مواد پیچیده به خواص فیزیکی ساخته در ساختار پلیمری و ترکیب فیزیکی حاصل در فاز رقیق و متراکم بستگی دارد.
تکنیکهای پراکندگی درجا روابط ساختار-عملکرد در مواد PEC و بایوساید ها را امکانپذیر کرده است که ممکن است به سؤالات بیوفیزیکی حلنشده در فرآیندهای سلولی بپردازد و همچنین توسعه مواد جدید را برای کاربردهای متنوع تسریع کند.
ما آمادهسازی مواد PEC با ویژگیهای پلیمری کنترلشده (طول، بلوک بودن، چگالی بار)، تکنیکهای پراکندگی اشعه ایکس با زاویه کوچک (SAXS) را که برای بررسی مقیاسهای طول مناسب و روالهای تحلیل دادهها از نقطهنظر عملی برای کاربران جدید استفاده میشوند، توصیف میکنیم. این مقاله به کمپلکس های توده ای می پردازد و نه به حوزه مرتبط، مهم و جالب مونتاژ غیرتعادلی لایه به لایه پلی الکترولیت ها.
پلی الکترولیت به چه معناست؟
پلی الکترولیت پلیمری از الکترولیت ها با چندین واحد زنجیره تکرار شونده است. این پلی الکترولیت ها دارای خواص الکترولیت و پلیمر هستند و وزن مولکولی بالایی دارند. با توجه به این موضوع و این واقعیت که پلی الکترولیت ها از یک نوع بار زیر واحد مونومر تشکیل شده اند، اغلب برای کاهش یا جلوگیری از خوردگی روی سطوح زیرلایه فلزی استفاده می شوند.

شکل 2. جداسازی میکروفاز PEC 1.69 با میکروسکوپ در حالت های DIC (سمت چپ) و فلورسانس (راست) فاز کواسروات (a, b) و فاز رقیق (c, d) نشان داده شده است که بالاتر از دمای تعادل (دمای اتاق) گرفته شده است. میله های مقیاس 100 میکرومتر هستند.

شکل 3. کدورت در برابر دمای فازهای کواسروات (دایره های آبی) و رقیق (الماس قرمز) PEC 1.69 . نمادهای جامد و خالی به ترتیب برای گرمایش و سرمایش هستند. نرخ گرمایش/سرمایش 0.1 درجه سانتی گراد در دقیقه -1 بود.

شکل 4. محدوده دمایی برای جداسازی میکروفاز نمونه های کواسروات متعادل شده در دمای اتاق. میلههای شناور و ناحیه خاکستری دمای تقریبی را نشان میدهند که در آن جداسازی میکروفاز از سطح مشترک شروع میشود و در سراسر کواسروات پخش میشود.

شکل 5. (الف) وابستگی خطی KBr/PE (دایره های آبی) به [KBr] برای دوپینگ PSS/PDADMA، که در آن سطح دوپینگ، y ، = KBr/PE (برای [KBr] <0.6 M). دوپینگ PSS/PDADMA توسط NaCl با خط نقطه چین نشان داده شده است که از مرجع 39 است. (ب) KBr/PE به شکل PECOX (الماس های آبی) و به صورت PECOV (دایره های قرمز) و محلول یکنواخت که در آن PEC حل می شود (مربع های سبز). هنگامی که رژیم دوپینگ خطی به y = 1.00 برون یابی می شود، [KBr] = 1.80 M. مرزهای بین حالت های مایع شیشه ای، لاستیکی، و الاستیک تیز نیستند.

شکل 6. نسبت مولی PSS/PDADMA (نمادهای جامد) و [PE] (نمادهای باز) در فازهای رقیق (مربع آبی) و کواسروات (دایره های قرمز) با 1H NMR. الماس سبز نسبت PSS/PDADMA را در محلول (یکنواخت) نشان می دهد.

شکل 7. نمودار فاز سه تایی برای ترکیبات تعادلی در درصد وزنی PSS/PDADMA PE، KBr و آب در فاز رقیق (○)، فاز کواسروات (◇)، و PECOX (Δ). خط جامد 2 O % wt در مقابل KBr wt % است: H 2 O % = 2.38 KBr % + 32 ( r 2 = 0.958). این خط از محور PE % در PE % 68% عبور می کند، که به این معنی است که هشت مولکول آب با هر جفت PSS/PDADMA ترکیب است.

شکل 8. مدول دینامیکی G ‘ (●)، G ″ (▲)، و η (■) در 0.1 هرتز، تنش برشی 25 Pa برای PSS/PDADMA با افزایش [KBr]. میانگین ویسکوزیته PDADMA خالص و PSS در [KBr] مناسب، که زنجیرههای جفت کاملا غیریونی را نشان میدهند، به صورت ضربدری نشان داده شدهاند.

شکل 9. محاسبه [KBr] حیاتی برای انحلال PEC به عنوان تابعی از درجه پلیمریزاسیون، DP، پلی الکترولیت ها.

کاربرد های پلی الکترولیت
پلی الکترولیت ها کاربردهای زیادی دارند که بیشتر مربوط به اصلاح جریان و خواص پایداری محلول ها و ژل . به عنوان مثال، آنها می توانند برای بی ثبات کردن یک سوسپانسیون کلوئیدی و برای شروع لخته (بارش) استفاده شوند. آنها همچنین می توانند برای انتقال بار سطحی به ذرات خنثی استفاده شوند و آنها را قادر می سازد در محلول آبی پراکنده شوند.
بنابراین اغلب به عنوان غلیظ کننده ، امولسیفایر ، حالت ، شفاف کننده و حتی کشش استفاده می شود. آنها در تصفیه آب و برای بازیافت روغن استفاده می شوند. بسیاری از صابون ها، شامپوها و لوازم آرایشی دارای پلی الکترولیت هستند. علاوه بر این، آنها به بسیاری از غذاها و به بتن ( فوق روان ) اضافه می شوند. برخی از پلی الکترولیت هایی که روی برچسب مواد غذایی ظاهر می شوند عبارتند از: پکتین ، کاراگینان ، آلژینات ها و کربوکسی متیل سلولز . همه به جز آخرین منشاء طبیعی دارند. در نهایت در مواد مختلفی از جمله سیمان استفاده می شود.
از آنجا که برخی از آنها محلول در آب هستند، برای کاربردهای بیوشیمیایی و پزشکی نیز مورد بررسی قرار می گیرند. در حال حاضر تحقیقات زیادی در مورد استفاده از زیست سازگار پلی الکترولیت های ایمپلنت ، انتشار کنترل دارو و سایر کاربردها وجود دارد. بنابراین، اخیراً، مواد درشت متخلخل زیست سازگار و زیست تخریب پذیر متشکل از کمپلکس پلی الکترولیت توصیف است، جایی که این ماده تکثیر عالی سلولهای پستانداران و محرکهای نرم مانند ماهیچهها را نشان میدهد.
پلی الکترولیت ها کاربردهای زیادی دارند که بیشتر مربوط به اصلاح جریان و بهبود پایداری کلوئیدها و ژل های آبی یا برای القای تجمع. به عنوان مثال، آنها می توانند برای بی ثبات کردن یک سیستم تعلیق کلوئیدی استفاده شوند و برای شروع لخته سازی و بارش. آنها همچنین می توانند برای ایجاد بار سطحی به ذرات خنثی مورد استفاده قرار گیرند و آنها را قادر می سازد تا در آنها پراکنده شوند یک محلول آبی بنابراین اغلب به عنوان استفاده می شوند غلیظ کننده ها، امولسیفایرها عوامل ، نرم ، کننده ها ، مبدل های یونی و عوامل روشنگر .
به عنوان مثال، آنها در آب استفاده می شوند درمان به عنوان عوامل لخته سازی، در دوغاب های سرامیکی به عنوان عوامل تثبیت کننده و در مخلوط بتن به عنوان فوق روان کننده علاوه بر این، بسیاری از شامپوها، صابون ها و لوازم آرایشی حاوی پلی الکترولیت هستند. پلی الکترولیت های خاصی نیز به محصولات غذایی اضافه می شوند. به عنوان مثال، به عنوان پوشش های غذایی و عوامل رهاسازی به عنوان مثال می توان به پکتین (اسید پلی گالاکترونیک)، آلژینات (اسید آلژینیک) و کربوکسی متیل سلولز اشاره کرد. همه به جز آخرین منشاء طبیعی دارند.
از آنجایی که پلی الکترولیت ها محلول در آب هستند، از آنها نیز استفاده می شود کاربردهای بیوشیمیایی و پزشکی مانند پوشش های ایمپلنت و سیستم های رهایش داروی کنترل.
مزایای پلی الکترولیت ها
پلی الکترولیت ها پلیمرهایی با گروه های تفکیک کننده در خود هستند واحدهای تکرار آنها را می توان به تقسیم کرد پلی کاتیون ها و پلی آنیون ها و پلی نمک ها . مانند الکترولیت های معمولی (اسیدها، بازها و نمک ها)، آنها در محلول های آبی (آب) تجزیه می شوند و مقدار pH یک یا چند بار را تحمل می کنند. بنابراین، خواص پلی الکترولیت ها هم مشابه الکترولیت ها و هم پلیمرها است. نمک ها، یعنی محصولات یک پلی اسیدها (پلی یون ها) با پایه مونومر و بالعکس، پلی نمک می شوند. مانند نمک های معمولی، محلول های آنها رسانای الکتریکی هستند و مانند پلیمرها، ویسکوزیته آنها قوی است. بستگی به وزن مولکولی و غلظت پلیمر دارد.
سه مورد از رایج ترین گروه های آنیونی کربوکسیلات (–COO- ) ، فسفونات (–PO 3 H- ، –PO 3 2- ) هستند. و سولفونات (-SO 3 – ) و رایج ترین گروه های کاتیونی آمونیوم اولیه، ثانویه و چهارتایی هستند (-NH 3 + , =NH 2 + و ≡N + ). در نوع گروه یونی، یون ضد آن و ساختار آن واحد تکرار خواص یک پلی الکترولیت مانند حلالیت در آب و سایر مایعات قطبی و پیوند هیدروژنی (الکل ها و غیره) را تعیین می کند. هدایت الکتریکی و ویسکوزیته محلول برخلاف غیریونیک پلیمرها، این خواص به شدت به pH و نمک بستگی دارد محتوا.
پلی الکترولیت ها را می توان با ترکیب a به صورت شیمیایی به هم متصل کرد مقدار کمی از یک عامل اتصال عرضی مناسب. این پلی الکترولیت ها ساختارهای سه بعدی را تشکیل می دهند که به جای حل شدن در آب، در آب متورم می شوند. آنها می توانند (به شدت) مقادیر زیادی مایع را نسبت به جرم خود از طریق پیوند هیدروژنی با مولکول های آب حفظ کنند. هیدروژل ها یا پلیمرهای سوپرجاذب (SAP’s) هنگامی که (کمی) پیوند متقابل دارند. توانایی آنها در جذب آب عاملی از غلظت یونی محلول آبی است. در آب دیونیزه و مقطر، SAPs می توانند تا 500 برابر وزن خود و 30 تا 60 آب جذب کنند بار خودشون حجم، یعنی یک هیدروژل می تواند از بیش از 99٪ مایع تشکیل باشد. ظرفیت جذب و تورم کل SAPها توسط نوع و کنترل می شود مقدار اتصالات عرضی در ساختار.
انواع پلی الکترولیت
پلی الکترولیت ها معمولاً هدف اولیه کاربردشان به سه نوع زیر واحد تقسیم می شوند. این واحدها عبارتند از:
- چند پلیکیشن ها
- پولیانیون ها
- پلی نمک ها
آنها به طور مشابه به الکترولیت های معمولی (اسیدها، بازها و نمک ها) تقسیم می شوند. با این حال، خروجی یک پلی اسید (پلی یون) با پایه مونومر و بالعکس، پلی نمک می شود. مانند نمک های معمولی، آنها رسانای الکتریکی هستند اما به دلیل ماهیت پلیمری خود بسیار چسبناک هستند.
خوردگی فولادهای خاص در شرایط آندی را می توان با اعمال لایه ای از کمپلکس پلی الکترولیت درمان کرد. در مطالعات تحقیقاتی، اسکنها روی یک ناحیه بستر مستعد خوردگی گسترده و اندازهگیریها در ناحیه حفرهای، درجه بالایی از اثربخشی چند لایه پلیالکترولیت را نشان میدهد که با مقاومت در برابر رطوبت و کنترل خوردگی، علیرغم نفوذپذیری یون مشخص میشود.
پلی الکترولیت های طبیعی و مصنوعی
هر دو بر روی یک می شوند در مقیاس بزرگ پلی الکترولیت های طبیعی رایج پکتین هستند (اسید پلی گالاکترونیک)، آلژینات (اسید آلژینیک)، کربوکسی متیل سلولز و پلی پپتید نمونه هایی از مصنوعی رایج پلی الکترولیت ها پلی اکریلیک اسید، پلی استایرن سولفونات، پلی آلی آمین، کربوکسی متیل سلولز و نمک های آنها. برخی از این پلی الکترولیت ها در زیر نشان داد:
برخی دیگر از پلی الکترولیت ها بر خلاف گروه های جانبی باردار حاوی گروه های باردار در زنجیره اصلی هستند. این دسته از پلی الکترولیت ها معمولاً به عنوان پلی یونن . رایج ترین گروه باردار در ستون فقرات آمونیوم چهارتایی است. این پلی آمین های یونی معمولاً از طریق واکنش منشوتکین آمین های درجه دوم سنتز می شوند. آلکیل دی هالیدها
تعداد زیادی از دی هالیدها و آمین های ترشیاری به صورت تجاری تولید می شوند موجود است که اجازه سنتز تعداد زیادی از به خوبی تعریف را می دهد پلی یونن ها از مواد اولیه نسبتا ارزان و نسبی مسیر سنتز ساده هر دو فاصله یونی روی ستون فقرات پلیمری، یعنی چگالی بار و وزن مولکولی را می توان به راحتی تنظیم کرد. علاوه بر این، بسیاری از گروه های کاربردی دیگر را می توان به راحتی گنجاند است، که اجازه می دهد تا برای اتصال عرضی و خیاطی خواص فیزیکی و مکانیکی
خواص فیزیکوشیمیایی
خواص پلی الکترولیت ها در محلول توسط برهمکنش الکترواستاتیکی بین گروه های باردار در زنجیره و یون های با وزن مولکولی کم در محلول میدان الکترواستاتیک قوی ایجاد توسط بارهای موجود در پلی الکترولیت تأثیر قابل توجهی بر ساختار مولکول دارد، یعنی به طور قابل ملاحظه ای ترکیبات ماکرومولکولی را تغییر می دهد. با افزایش درجه تفکیک، اندازه مؤثر زنجیرهها (فاصله انتها به انتها، شعاع هیدرودینامیکی و غیره) افزایش مییابد و مولکولهای مارپیچ صاف میشوند و تقریباً خطی میشوند. شکل چوب مانند در درجات بالایی از تفکیک پلی الکترولیت.
خواص فیزیکوشیمیایی دستخوش تغییرات قابل توجهی می شود زمانی که درجه تفکیک تغییر می کند. به عنوان مثال، ویسکوزیته محلول می تواند یک عامل افزایش یابد از صد یا بیشتر غلظت پلی الکترولیت در محلول، درجه تفکیک آن و غلظت یون آزاد (نمک) (یونهای با وزن مولکولی کم در محلول).
نظریه ای که برای راه حل های توسعه الکترولیت های با وزن مولکولی کم برای پلی الکترولیت معتبر نیستند راه حل ها یون های با وزن مولکولی کم که در طول دوره ظاهر می شوند تفکیک گروه های قطبی پلی الکترولیت ها ایجاد الف ابر ضد یون منتشر در اطراف سطح دارای بار مخالف پلیمرها ترکیب (انحلال پذیری) و اندازه آن بر ساختار و دینامیک پلی الکترولیت ها تأثیر می گذارد در محلول و همچنین ظرفیت تورم و پاسخ ویسکوالاستیک ژل های پلی الکترولیت.
زنجیره های مولکولی باردار معمولاً وجود دارند در سیستم های ماده نرم تأثیر قابل توجهی بر ساختار دارند، پایداری و برهمکنشهای مجموعههای مولکولی مختلف (بیولوژیکی). رویکردهای نظری برای توصیف ویژگی های آماری آنها به شدت با خنثی الکتریکی آنها متفاوت است همتایان بسیاری از مولکول های بیولوژیکی پلی الکترولیت هستند. به عنوان مثال، پلی پپتیدها و DNAها پلی الکترولیت هستند.
| پلی الکترولیت | ساختار واحد تکرار | نام تجاری |
| پلی اکریلیک اسید (PAA) | Acusol (کوپلیمر)، Acumer، Acrysol، Alcosperse | |
| پلی استایرن سولفونات | Resonium، Sorbisterit، Resikali |
برخی از پلی الکترولیت ها و ماهیت یونی آنها
| نوع پلی الکترولیت | پولیانیون ها | چند پلیکیشن ها |
|---|---|---|
| طبیعی |
|
|
| اصلاح شیمیایی/نیمه مصنوعی |
|
|
| مصنوعی |
|
|
عوامل موثر بر سنتز هیدروژل های مجتمع پلی الکترولیت
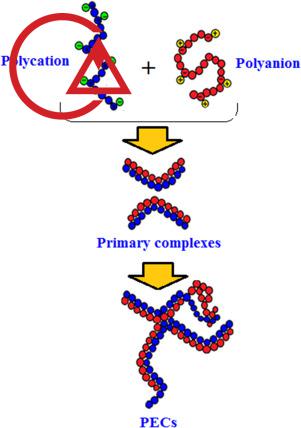
هنگامی که پلیمرهای کاتیونی با پلیمرهای آنیونی در محلول آبی، حتی در محلول های رقیق، مخلوط می شوند، PEC ها را می توان به صورت رسوب به دست آورد ( Huguet et al., 1994 ). تشکیل PEC ها را می توان به سه مرحله تقسیم کرد: کمپلکس اولیه، درون کمپلکس و بین کمپلکس. نیروی اتصال اولیه در تشکیل PECها نیروهای کولن است.
یک مرحله میانی شامل تشکیل پیوندهای جدید و/یا اصلاح اعوجاج زنجیره پلیمری است. در نهایت، تجمع کمپلکس های ثانویه عمدتاً به دلیل فعل و انفعالات آبگریز اتفاق می افتد ( Tsuchida, 1994 ). سنتز پلی الکترولیت – ذرات هیدروژل زیست پلیمری را می توان با در نظر گرفتن CS به عنوان یک پلی الکترولیت کاتیونی و ALG به عنوان یک پلیمر زیستی نشان داد. ذرات هیدروژل PEC را می توان با ریختن محلول ALG در محلول کلرید کلسیم و سپس انتقال کلسیم ALG به محلول CS در اسید استیک برای تشکیل غشای پیچیده روی سطح ذرات تهیه کرد.
ذرات دارای یک هسته ALG و یک غشای پیچیده ALG-CS نیز می توانند در فرآیند یک مرحله ای، به سادگی با افزودن قطرات ALG به محلول CS شوند. هوگت و دلاچری، 1996 ). بر خلاف این، ریختن محلول CS به ALG می تواند ذرات با هسته CS را ایجاد کند که توسط غشای CS-ALG PEC احاطه است ( Daly and Knorr, 1988 ). تشکیل PECها تحت تأثیر خواص شیمیایی مانند pH، چگالی بار، وزن مولکولی و همچنین شرایط تجربی مانند غلظت پلی الکترولیت ها، نسبت اختلاط آنها، قدرت یونی محلول و موارد دیگر است. تأثیر pH بر تشکیل کمپلکس بسیار مهم است و ممکن است بر عملکرد کمپلکس و نفوذپذیری غشاهای پیچیده تأثیر بگذارد. از آنجایی که ذرات PEC با برهمکنش یونی تشکیل می شوند، چگالی بار هر دو الکترولیت مهم است. با این حال، pH یک محلول میتواند بار و چگالی بار حاکم بر ماکرومولکولهای شرکتکننده را تغییر دهد.
کمپلکس در مقادیر pH بالاتر سریعتر حل می شود.
همانطور که چگالی اتصال متقابل بر خواص هیدروژل های دارای پیوند متقاطع حاکم است، خواص PEC ها عمدتاً توسط میزان برهمکنش بین پلیمرها تعیین می شود. در واقع، هرچه چگالی بار پلیمر کمتر باشد، نسبت پلیمر در PEC بیشتر است، زیرا زنجیره های پلیمری بیشتری برای واکنش با پلیمر دیگر مورد نیاز است ( برگر و همکاران، 2004 ). Simsek-Ege و همکاران. (2003) اثر pH را بر تشکیل CS-ALG PEC مطالعه کرد. رسوب CS در pH> 6.0 و ALG در pH <3.6 رسوب مشاهده شد. ALG از اسید گولورونیک (M) و Yalpani که مقادیر pK a به ترتیب 3.38 و 3.65 است ( and Hall, 1984 ). بازده مجتمع در pH 5 بالاتر از آنچه در pH 2 است، که می تواند مربوط به کربوکسیلیک اسید در سطح ALG باشد، بیشتر بود.
شایان ذکر است که بار سطحی مثبت روی ذرات به دلیل ویژگیهای کاتیونی CS و درجه بالای استیلزدایی آن (95%) بیشتر میشود. افزایش غلظت هر کدام پلی کاتیون یا پلی آنیون ممکن است به اندازه بزرگتر ذرات PEC منجر شود. در غلظتهای بالاتر پلیالکترولیت، تعداد مولکولهای در هم به شدت افزایش مییابد و اندازه ذرات افزایش مییابد. معمولاً، پلی الکترولیت های با مگاوات کم به زمان کوتاهتری برای اختلاط و تشکیل PECهای کوچکتر نیاز دارند. پلی الکترولیت های با مگاوات بالا به زمان بیشتری برای اختلاط نیاز دارند تا PEC هایی با اندازه بزرگ تشکیل دهند. با افزایش نسبت اختلاط، پایداری کلوئیدی ممکن است به طور ناگهانی کاهش یابد ( Ankerfors et al., 2010 ). تغییر قدرت یونی با افزودن نمک می تواند برهمکنش های الکترواستاتیکی را در محلول پلی الکترولیت تعدیل کند ( الکساندر و مونیکا، 2004 ). غلظت نمک بالاتر باعث کاهش پایداری PEC و کاهش چگالی بار می شود.
خواص فیزیکی وشیمیایی
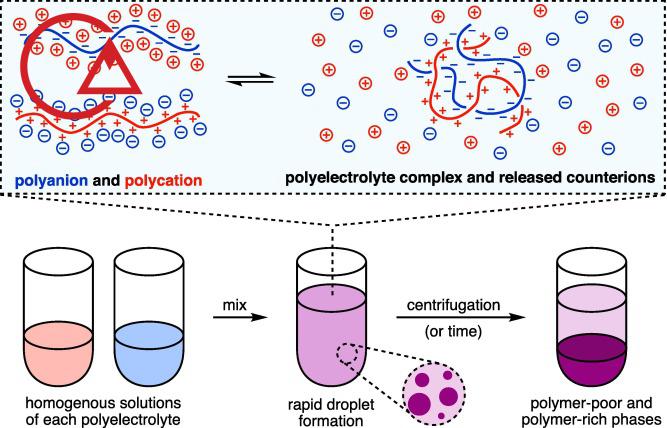
پلی الکترولیت به عنوان یک ابزار نوآورانه، ساده و امیدوارکننده برای ارائه و هدف قرار دادن مواد زیست فعال درمانی پدید آمده اند. پلیالکترولیتها توانایی تشکیل مجتمعها/نانو کمپلکسها را با مواد پلیمری با بار مخالف یا بیوماکرومولکولها دارند و به همین دلایل منجر به کاربردهای مختلفی در بخش زیستپزشکی و صنایع داروسازی و (نانو) بیوتکنولوژی شدهاند. پلیالکترولیتها پلیمرها یا کوپلیمرهای هستند که حامل گروههای قابل یونیزاسیون هستند و هنگام آزاد کردن یونهای کوچک، که اغلب یونهای متضاد نامیده میشوند ، در محیط پراکندگی حلال اطراف، باردار میشوند ( Odijk, 1979; Sogami and Ise, 1984; Förster et al., 1992; بارات و جوانی، 1996؛ موتوکومار، 1997 ). خواص فیزیکوشیمیایی آنها به توزیع بار حمل در طول زنجیره، معماری زنجیره پلیمری (وزن مولکولی، خواص خودآرایی یا پدیده های سطحی ماکرومولکول) و البته ترکیب شیمیایی بستگی دارد.
در مورد پلیمرهای بدون گروههای یونیزاسیون (پلیمرهای بدون بار)، وزن مولکولی، معماری ماکرومولکولی یا شبکهای از زنجیرههای پلیمری در نظر گرفته میشود که تأثیر عمدهای بر خواص فیزیکوشیمیایی یک پلیمر خنثی در محیط محلول/آبی دارد. وجود هر گونه بار در محلول حجیم/محیط آبی اطراف ماکرومولکول/پلیمر زنجیره نقش کلیدی در تعیین خواص فیزیکوشیمیایی پلی الکترولیت ها ایفا می کند.
تفاوت بین خواص محلول پلی الکترولیت رقیق و نیمه رقیق با قدرت برهمکنش های بین مولکولی و درون مولکولی تعیین می شود. در یک محلول پلی الکترولیت نیمه رقیق، زنجیره های پلیمری با هم همپوشانی دارند و انفعالات بین مولکولی نقش عمده ای در تأثیرگذاری بر خواص سیال/مایع دارند. در محلول های رقیق، زنجیره های پلی الکترولیت پراکنده می شوند و برهمکنش های درون مولکولی خواص پراکندگی و رفتار نهایی سیستم های محلول را کنترل می کنند.
ساختار شیمیایی پلی الکترولیت
ساختارهای شیمیایی دو پلی الکترولیت مصنوعی، به عنوان مثال. در سمت چپ پلی (سدیم استایرن سولفونات) (PSS) و در سمت راست اسید پلی اکریلیک (PAA) قرار دارد. هر دو در صورت تفکیک پلی الکترولیت هایی با بار منفی هستند. PSS یک پلی الکترولیت “قوی” است (کاملاً در محلول شارژ می شود)، در حالی که PAA “ضعیف” است.
پلی الکترولیت ها پلیمرهایی که واحدهای تکرار شونده آنها دارای یک الکترولیت هستند. کاتیون ها و پلی آنیون ها پلی الکترولیت هستند. این گروه ها تجزیه در محلول و پلیمرها را شارژ می کنند. بنابراین خواص پلی الکترولیت هم مشابه الکترولیت ها ( نمک ها ) و هم پلیمرها ( وزن مولکولی ) است و گاهی اوقات پلی نمک . مانند نمک ها، محلول های آنها رسانای الکتریکی هستند. مانند پلیمرها، محلول های آنها اغلب چسبناک هستند.
زنجیرههای مولکولی باردار، که معمولاً در سیستمهای ماده نرم وجود دارند، نقش اساسی در تعیین ساختار، پایداری و برهمکنشهای مجموعههای مولکولی مختلف دارند. رویکردهای نظری [1] برای توصیف خواص آماری آنها عمیقاً با همتایان خنثی الکتریکی آنها متفاوت است، در حالی که زمینه های فنی و صنعتی از ویژگی های منحصر به فرد آنها استفاده می کنند. بسیاری از مولکول های بیولوژیکی پلی الکترولیت هستند. به عنوان مثال، پلی پپتیدها ، گلیکوزآمینوگلیکان ها و DNA پلی الکترولیت هستند. هر دو پلی الکترولیت طبیعی و مصنوعی در صنایع مختلفی استفاده می شوند.
پلی الکترولیت: پلیمر متشکل از ماکرومولکول هایی که در آن بخش قابل توجهی از واحدهای تشکیل دهنده شامل گروه های یونی یا قابل یونیزاسیون یا هر دو است.
- اصطلاحات پلی الکترولیت، الکترولیت پلیمری و الکترولیت پلیمری را نباید با واژه الکترولیت پلیمری جامد اشتباه گرفت.
- پلی الکترولیت ها می توانند مصنوعی یا طبیعی باشند. اسیدهای نوکلئیک، پروتئین ها، اسیدهای تیکوئیک، برخی پلی پپتیدها و برخی پلی ساکاریدها نمونه هایی از پلی الکترولیت های طبیعی هستند.
ترکیب پلی الکترولیت
ترکیب هر پلیمر تحت تأثیر عوامل متعددی قرار می گیرد: به ویژه معماری پلیمر و میل ترکیبی حلال. در مورد پلی الکترولیت ها شارژ نیز تاثیر دارد. در حالی که یک زنجیره پلیمری خطی بدون بار معمولاً در یک ترکیب تصادفی در محلول یافت می شود (تقریباً یک پیاده روی تصادفی یکدیگر را دفع می نیروهای دو لایه که باعث می شود زنجیره یک ترکیب میله مانند گسترش تر را اتخاذ کنید. اگر محلول حاوی مقدار زیادی نمک اضافه باشد، بارها غربال می شوند و در نتیجه زنجیره پلی الکترولیت به یک ترکیب معمولی تر فرو می ریزد (که اساساً مشابه یک زنجیره خنثی در حلال ).
پلیمر ترکیب بر بسیاری از خواص توده ای (مانند ویسکوزیته ، کدورت و غیره) تأثیر می گذارد. اگرچه ترکیب آماری پلیالکترولیتها را میتوان با استفاده از انواع تئوری پلیمرهای مرسوم به دست آورد، به دلیل ماهیت دوربرد برهمکنش الکترواستاتیک، به طور کلی مدلسازی صحیح زنجیرههای پلیالکترولیت از نظر محاسباتی بسیار سخت است.
پلی آمفولیت ها
پلی الکترولیت هایی که دارای هر دو گروه تکرار کاتیونی و آنیونی هستند، پلی آمفولیت . رقابت بین تعادل اسید و باز این گروه ها منجر به عوارض اضافی در رفتار فیزیکی آنها می شود. این پلیمرها معمولاً تنها زمانی حل می شوند که نمک اضافه کافی وجود داشته باشد، که فعل و انفعالات بین بخش های دارای بار مخالف را بررسی می کند. در مورد هیدروژلهای ماکرو متخلخل آمفوتریک، عمل محلول نمک غلیظ منجر به انحلال مواد پلیآمفولیت به دلیل اتصال عرضی کووالانسی ماکرومولکولها نمیشود. هیدروژلهای ماکرو متخلخل مصنوعی سه بعدی توانایی عالی برای جذب یونهای فلزات سنگین در محدوده وسیعی از pH از محلولهای آبی بسیار رقیق را نشان میدهند، که بعداً میتواند به عنوان جاذب برای تصفیه آب شور استفاده شود 3] [4] همه پروتئینها [ پلی آمفولیت ها، زیرا برخی از اسیدهای آمینه تمایل به اسیدی دارند، در حالی که برخی دیگر بازی هستند.
- پلیمر آمفولیتیک : پلی الکترولیت متشکل از ماکرومولکول های حاوی هر دو گروه کاتیونی و آنیونی یا گروه قابل یونیزاسیون مربوطه. توجه داشته باشید:
- یک پلیمر آمفولیتیک که در آن گروههای یونی با علامت مخالف در همان گروههای آویز گنجاند ساختار گروههای آویز، یک . پلیمر زوئیتریونی، نمک داخلی پلیمری یا پلی بتائین میشود